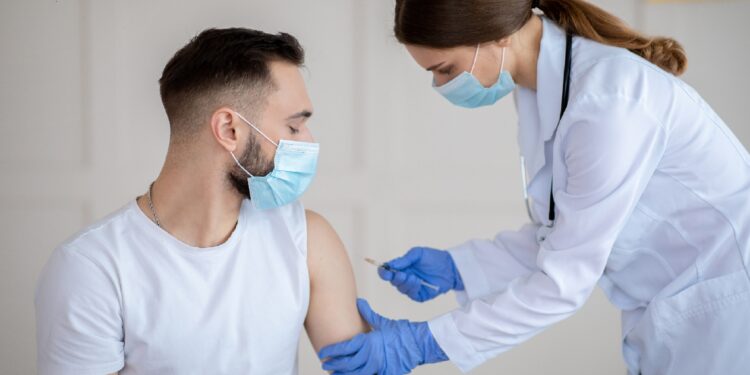
COVID-19-Impfung: Langfristige Aktivierung der Abwehrzellen
SARS-CoV-2-mRNA-Impfstoffe spielen eine Schlüsselrolle bei der Bekämpfung der anhaltenden COVID-19-Pandemie. Die Impfung stimuliert die Zellen des angeborenen Immunsystems, doch bisher war nicht bekannt, wie lange diese Wirkung andauert. Dazu haben Forschende jetzt neue Erkenntnisse gewonnen.
Wenn das menschliche Immunsystem in Kontakt mit dem Coronavirus SARS-CoV-2 kommt, wehrt es sich und bildet Antikörper. Eine ähnliche Immunantwort wird durch die Impfstoffe gegen COVID-19 ausgelöst. Zur Dauerhaftigkeit des Immunschutzes liegen bislang allerdings nur wenig Daten vor. Doch dazu gibt es nun neue Erkenntnisse: In der Fachzeitschrift „EMBO Molecular Medicine“ wurden kürzlich Studienergebnisse zur Aktivierung von Abwehrzellen nach der SARS-CoV-2-mRNA-Impfung veröffentlicht.
Guter Schutz gegenüber schweren Verläufen
Bei manchen Menschen führt eine Infektion mit SARS-CoV-2 zu schwersten Entzündungen der Lunge und anderer lebenswichtiger Organe. Die Corona-Impfung bietet einen sehr guten Schutz gegenüber diesen schweren Krankheitsverläufen.
Wie es in einer Mitteilung der Uniklinik Köln heißt, haben sich zahlreiche Studien mit der Rolle der sogenannten erworbenen Immunantwort nach der Impfung beschäftigt und konnten zeigen, dass beispielsweise Antikörper nach der Impfung im Blut zu messen sind und diese dann über Monate hinweg weniger werden.
Für das Auslösen einer potenten Immunantwort benötigen Impfungen aber zunächst die Aktivierung des angeborenen Immunsystems, das unspezifisch auf körperfremde Eiweiße von Viren oder Bakterien reagiert. Es war bisher nicht bekannt, wie genau und wie lange die neuen mRNA-Impfstoffe die Zellen des angeborenen Immunsystems stimulieren.
Forschende der Uniklinik Köln sowie der Medizinischen Fakultät fokussieren in der nun veröffentlichten Impfstudie erstmals auf die Signalwege dieser Abwehrzellen und deren Auswirkung auf die erworbene Immunantwort.
Wichtig für möglichst langanhaltende und potente Wirkung
Die schnelle Entwicklung von potenten Impfstoffen gegen das Coronavirus SARS-CoV-2 hat stark zur Eindämmung der Pandemie beigetragen. Zahlreiche Studien belegen den Schutz vor schweren COVID-19-Verläufen und eine Reduktion der Ansteckungen durch eine vollständige Impfung.
Insbesondere die potenten mRNA-Impfstoffe, die rasch zur Verfügung gestellt werden konnten, waren ein wichtiger Meilenstein für diese Entwicklung. Mittlerweile konnte von Forschenden relativ gut untersucht werden, wie lange der Impfschutz über eine Aktivierung des erworbenen Immunsystems anhält.
Wichtig für eine möglichst langanhaltende und potente Wirkung einer Impfung ist zunächst aber die Aktivierung des angeborenen Immunsystems, welches das Zusammenspiel von verschiedenen Abwehrzellen anstößt und eine Gedächtnisfunktion im Immunsystem hinterlässt.
Bei den meisten herkömmlichen Impfstoffen werden dafür sogenannte Adjuvantien genutzt, Zusatzstoffe, die Zellen des angeborenen Immunsystems wie beispielsweise Makrophagen anregen sollen. Bei mRNA-Impfstoffen fehlen diese klassischen Zusätze, und der Mechanismus, mit dem Abwehrzellen direkt nach der Impfung stimuliert werden, ist noch nicht bekannt.
Beobachtete Effekte nach zweiter Impfung besonders stark
Hier setzt die Forschung der Arbeitsgruppe von Priv. Doz. Dr. Dr. Jan Rybniker an. „Wir konnten zeigen, dass die mRNA-Impfung im Blut zirkulierende Makrophagen sehr spezifisch über einen ganz bestimmten Signalweg anregt“, erklärt der Wissenschaftler.
„Erst wenn diese Makrophagen mit dem Spike-Protein von SARS-CoV-2 in Kontakt kommen, erlaubt die Voraktivierung der Zellen die Ausschüttung entzündungsfördernder Botenstoffe und somit die Aktivierung von Abwehrzellen des erworbenen Immunsystems.“
Den Angaben zufolge stellt diese Voraktivierung der Blutzellen auch eine Art Schutzvorrichtung der Zellen dar, bei der erst im Spike-Protein produzierenden Gewebe eine Entzündung entsteht und eben nicht für längere Zeit im ganzen Körper.
Laut Rybniker, Leiter des Forschungslabors der Infektiologie an der Uniklinik Köln und Letztautor der Veröffentlichung, erfolgt diese Entzündungsreaktion dann am ehesten lokal begrenzt im Lymphknoten, in den diese Blutzellen einwandern können.
Die in der aktuellen Studie beobachtete, sehr spezifische Reaktion auf das Spike-Protein ist für Abwehrzellen des angeborenen Immunsystems ungewöhnlich. Verantwortlich hierfür sind demnach Spike-Protein bindende Rezeptoren auf der Oberfläche der Makrophagen. Diese Rezeptoren aktivieren nach der Impfung das zentrale Kontrollprotein SYK, das zahlreiche entzündungsfördernde Prozesse in den Abwehrzellen aktiviert.
Die beobachteten Effekte waren interessanterweise erst nach der zweiten Impfung besonders stark ausgeprägt. Doch auch die dritte Impfung (Booster) konnte noch Monate nach der Grundimmunisierung die Makrophagen reaktivieren. Im Blut vorliegende Makrophagen haben aber eine sehr kurze Lebensdauer von nur wenigen Tagen.
„Anscheinend führt die Grundimmunisierung auch zu einer Gedächtnisfunktion in diesen kurzlebigen Zellen. Diese wichtige Erkenntnis ist für die mRNA-Impfung neu. Der zugrundeliegende Mechanismus könnte ebenfalls zu der starken Schutzwirkung, die wir durch die Booster-Impfung erzielen, beitragen“, so Dr. Sebastian Theobald, Postdoktorand an der Uniklinik Köln und Erstautor der Studie.
Ergebnisse auch für künftige Impfungen zu nutzen
Der in der Arbeit beschriebene SYK-Signalweg und die vorgeschalteten Rezeptormoleküle gelten bereits seit längerer Zeit als ein möglicher und attraktiver Mechanismus, mit dem im Rahmen von Impfungen Zellen des angeborenen Immunsystems stimuliert werden könnten. Diese Theorie kann jetzt für die mRNA-Impfung, die ein sehr gutes Sicherheitsprofil aufweist, bestätigt werden.
Die Ergebnisse können nun genutzt werden, um auch bei zukünftigen Impfungen ganz gezielt ähnliche immunitätsverstärkende Mechanismen zu aktivieren, beispielsweise über entsprechende Adjuvantien.
„mRNA basierte Therapien und Impfungen sind auf dem Vormarsch. Umso wichtiger ist es bereits jetzt, möglichst viele Informationen über die durch diese Medikamente ausgelösten Immunantworten zu entschlüsseln um deren Potential voll auszuschöpfen“, sagt Dr. Rybniker.
Möglicher therapeutischer Ansatzpunkt
Der SYK-Signalweg scheint auch bei der schweren COVID-19 Erkrankung eine Rolle zu spielen. In einer früheren Studie konnte die Gruppe schon ähnliche Einflüsse auf Blutzellen von COVID-19-Patientinnen und -Patienten nachweisen.
Daher gilt SYK auch als ein möglicher therapeutischer Ansatzpunkt für immunmodulatorische Behandlungen bei schweren COVID-19-Infektionen. Es werden bereits klinische Studien mit entsprechenden Medikamenten durchgeführt. (ad)
Autoren- und Quelleninformationen
Dieser Text entspricht den Vorgaben der ärztlichen Fachliteratur, medizinischen Leitlinien sowie aktuellen Studien und wurde von Medizinern und Medizinerinnen geprüft.
- Uniklinik Köln: COVID-19-Impfung aktiviert langfristig das angeborene Immunsystem – Signalweg entschlüsselt, (Abruf: 05.07.2022), idw-online.de
- Sebastian J Theobald, Alexander Simonis, Julie M Mudler, Ulrike Göbel, Richard Acton, Viktoria Kohlhas, Marie-Christine Albert, Anna-Maria Hellmann, Jakob J Malin, Sandra Winter, Michael Hallek, Henning Walczak, Phuong-Hien Nguyen, Manuel Koch, Jan Rybniker: Spleen tyrosine kinase mediates innate and adaptive immune crosstalk in SARS-CoV-2 mRNA vaccination; in: EMBO Molecular Medicine, (veröffentlicht: 04.07.2022), EMBO Molecular Medicine
Wichtiger Hinweis:
Dieser Artikel enthält nur allgemeine Hinweise und darf nicht zur Selbstdiagnose oder -behandlung verwendet werden. Er kann einen Arztbesuch nicht ersetzen.